《Nature》子刊最新论文:CRISPR基因编辑技术导致小鼠体内上百种非目标基因突变
近年来,CRISPR技术被越来越多的人认为是癌症的“控制中心”,可以用来修复导致失明的基因突变、治疗生物的遗传疾病、甚至通过编辑人类胚胎基因来找出导致不孕和流产的原因。
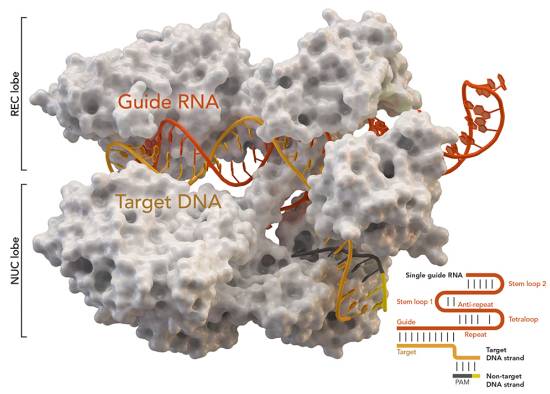
近日,Nature 子刊 Nature Methods 发表的一篇文章则表明,基因编辑技术有可能会在引起基因组内数百种尚不确定的基因突变。
“我们一致认为,CRISPR引起的偏靶突变这一发现具有非常严重的潜在危害,其中包括单核苷酸突变和基因组非编码区域的突变。”论文联合作者、哥伦比亚大学医学中心的 Stephen Tsang 博士说。

众所周知,CRISPR-Cas9基因编辑技术凭借其快速和高精确度的特点,被科学家视为了解基因在疾病中作用的重要途径。与此同时,基因编辑技术由于可以删除或修复有缺陷的基因,所以它也为基因治疗带来了新的希望。
世界上首例将CRISPR应用于人体的治疗案例目前正在中国进行,而欧美国家也会很快跟上。甚至有专家认为,目前中美在该领域的竞争将日趋白热化,有点类似当初冷战时期的美苏太空竞赛,只不过这次的主题换成了生物医疗。
然而,看似前景无可限量的 CRISPR 技术却也遭到了质疑。研究人员已经发现了该技术在用于活体生物时可能产生副作用的证据,而且其导致的非目标基因突变有可能将远远超出我们的想象。
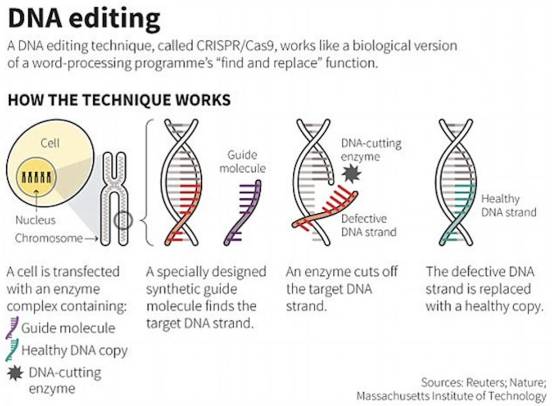
在之前的研究中,Tsang 博士和他的研究团队对两只 CRISPR 基因编辑的小鼠做了全基因组测序,并进行了健康程度比对。他们试图找到 CRISPR 引起的突变,包括合成 DNA 和 RNA 最基本的单核苷酸分子。
他们发现,CRISPR基因编辑技术确实成功修复了小鼠体内导致失明的基因,但这两只小鼠体内却出现了超过 1500 个单核苷酸位点变异(SNVs),以及超过 100 个大片段序列插入与缺失(InDels)。
“研究者们经常会使用一些计算机算法来预测非目标 DNA 突变,然而小鼠体内发生的这些突变从来没有被预测到”,Tsang 研究团队的报告指出。
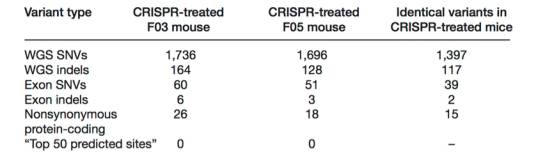
在上面图表的前两行,即全基因组测序单核苷酸位点变异(WGS SNVs)与全基因组测序大片段序列插入与缺失(WGS indels),已经说明了 CRISPR 基因编辑小鼠体内产生的非目标突变。
巴苏克博士表示:“虽然我们对 CRISPR 依旧保持乐观,但作为医生,我们知道任何一种新的疗法都会有潜在的副作用,而对于 CRISPR,我们也必须要找出它的副作用是什么。”
但与众多科学实验一样,小鼠体内发生的突变不一定意味着人体实验无法开展,只是现在的当务之急是要确定这类突变是否会在更大规模、更复杂的样本中出现,比如人体。
目前,研究人员也在积极改进 CRISPR 系统中基因切割酶和将酶引导到正确基因的 RNA 的部分,以此来提高基因编辑的效率。
Tsang 博士进一步补充道:“我希望,我们的研究结果可以促使其他人使用全基因组测序来作为判断他们所研究的 CRISPR 技术的脱靶效应,进而筛选出最安全、最准确的基因编辑技术。”
据《自然》杂志早些时候的报道,2016年10月28日,由肿瘤学家卢铀教授领导的四川大学的研究团队在华西医院将经过基因编辑的细胞注入到了一名参与临床试验的肺癌患者体内。
中国科学家主导的人体试验原本计划于 2016 年 8 月进行,但由于培养被编辑的细胞所需要的时间超出了最初的预期,所以才一直拖到十月底。不过中国在 CRISPR 技术上的应用上的步伐已经远远走在了美国前面。

美国的首次 CRISPR 人体试验目前还处于计划阶段。虽然在 2016 年初,美国的研究人员就已经获准进行此项试验,并且获得了科技大亨肖恩·帕克(Sean Parker)的投资,但估计一直要等到 2017 年晚些时候,这项试验才会在宾夕法尼亚大学进行。

正如宾夕法尼亚大学肿瘤细胞免疫疗法专家、美国首例CRISPR人体实验科学顾问Carl June所说:“我认为在生物医学领域上将爆发一场新的‘美苏太空竞赛’,不过这次的竞争双方将是中国和美国。不过竞争也是很重要的,因为它通常有助于提高最终技术的可靠性。”


